化学品の分類についての基礎的な知識及び通則を確認をしましょう。
化学品を分類する上でまず第一に考える事は
化学的に単一か、混合物か?
単一とは化学的に単一で、1つの化学式で表せるもので単一は、28類又は29類に分類される。
混合物(調製品)とは用途によって30類から38類に分類される。
28類又は29類に分類されるもの(化学的に単一とみなすもの)は下記の物質である。
・水溶液
・不純物を含むもの
・水以外の溶媒に溶かしたもの
・安定剤を加えたもの
・香気性物質、若しくは、催吐剤を加えたもの
化学品における例外規定がある。
①優先的に分類されるもの
②科学的に単一でも28類と29類に分類されないもの
③炭素の化合物だが28類に分類されるもの。
上から順番にあてはめて分類をする。
次に、①から順番に説明致します。
①優先的に分類されるもの
放射性元素及び放射性同位元素
同位元素及びその無機又は有機の化合物
貴金属の無機又は有機の化合物
希土類金属、イットリウム又はスカンジウムの化合物
水銀化合物
下記の動画でもお楽しみ下さい。
29類有機化合物の化学品における例外規定二つ目、科学的に単一だが28類や29類へ分類されないもの。
主に用途が優先される物質や製品など。以下一覧となっています。
| 分類番号 | 品名 |
|---|---|
| 2201項 | 水(海水は 2501、純水は 2853、重水は 2845 項) |
| 17類 | 甘味料(ショ糖、ぶどう糖、果糖、麦芽糖、乳糖) |
| 2501項 | 塩(塩化ナトリウム(NaCl)) |
| 3004項~3006項 | 投与量・小売用にした医薬品及び免疫産品 |
| 2519項 | 酸化マグネシウム(MgO) |
| 31類 | 肥料(硝酸ナトリウム、硝酸アンモニウム、尿素、塩化カリウム、硫酸アンモニウム等) |
| 3212項 | 小売用の形状又は包装にした染料、その他の着色料 |
| 3506項 | 小売用にした正味重量1kg以下の膠着剤・接着剤 |
| 2207項~2208項 | エチルアルコール(酒)(CH₃CH₂OH) |
| 3707項 | 小売用の写真用品(※塩化銀は 2843) |
| 2711項 | メタン及びプロパン(燃料)(CH₄、CH₃CH₂CH₃) |
| 3824項 | 培養単結晶(アルカリ金属、アルカリ土類金属のハロゲン化物で1個の重量が2.5g以上のもの) |
| 3507項 | 酵素 |
| 3818項 | 元素を電子工業用にドープ処理したもの(円盤状、ウェハー状その他の形状に切ったもの) |
| 3203項 | 植物性又は動物性の着色料 |
| 3204項 | 有機合成着色料、ルミノホアとして使用する種類の合成した有機物、蛍光増白剤 |
| 3206項 | ルミノフォアとして使用する種類の無機物 |
| 3207項 | ガラスフリットその他のガラスで粉状、粒状又はフレーク状のもの |
| 3606項 | たばこ用のライターの燃料 |
| 1504項~1520項 | 粗いグリセリン |
| 3813項 | 消火用に装てんした物品 |
| 3824項 | 小売用のインキ消し |
下記の動画でもお楽しみ下さい。
29類有機化合物の化学品における例外規定三つ目は炭素の化合物だが、28類へ分類されるもの。
有機化合物と無機化合物で、単一の物質を分類する上で大切なポイントとは
有機化合物か無機化合物かの確認であり、その単一の物質に、炭素が含まれなければ、無機化合物(28類)へ炭素を含めば有機化合物(29類)へ分類される。
有機化合物か、無機化合物かを見分けるポイントとは
無機化合物、は炭素を含まない、28類へ分類
有機化合物、は炭素を含む、29類へ分類
炭化水素を骨格とする化合物、炭化水素とは、炭素と水素だけで構成される化合物です。
炭素を含んでいるが28類に分類されるもの、主な品物は次の通りです。
| 品目 | 例 | 項 |
|---|---|---|
| 炭素の酸化物 | 一酸化炭素(CO) | 2811 |
| 炭素の酸化物 | 二酸化炭素(CO₂) | 2811 |
| 炭素の硫化物 | 二硫化炭素(CS₂) | 2813 |
| 炭化物 | 炭化カルシウム(CaC₂) | 2849 |
| 無機シアン系化合物 | シアン化水素(HCN) | 2811 |
| 無機シアン系化合物 | ジシアン(NC–CN) | 2853 |
| 無機シアン系化合物 | シアナミド(H₂N–CN) | 2853 |
| 炭酸塩 | 炭酸アンモニウム((NH₄)₂CO₃) |
下記の動画でもお楽しみ下さい。
周期律と電子配置
電子の並び方(電子配置)は周期的に変化し、これが元素の性質の周期性を生む。電子はエネルギーの低い殻から順に入っていき、K殻には2個、L殻には8個、M殻には18個、N殻には32個まで入る。ただし実際には途中で外側の殻に電子が入ることもある。たとえば塩素(原子番号17)は K殻に2個、L殻に8個、M殻に7個の電子を持つ。
原子の中心(原子核)
●
そのまわりを電子が回るイメージ
K殻| ●● | 2個
L殻| ●●●●●●●● | 8個
M殻| ●●●●●●●●●●●●●●●●●● | 18個
例:塩素(17個)
K殻:●●
L殻:●●●●●●●●
M殻:●●●●●●●
遷移元素の特徴
周期表の4周期以降の3〜12族にある金属は遷移元素と呼ばれ、価電子が1〜2個で隣同士の元素が似た性質を示す。すべて金属であり、有色のイオンや化合物をつくりやすく、錯イオンを形成しやすい。電子殻の一部が埋まりきっていないため触媒として働きやすく、複数の酸化数をとることが多い。たとえば鉄(Fe)は2価(Fe²⁺)では酸化鉄(Ⅱ)(FeO)、3価(Fe³⁺)では酸化鉄(Ⅲ)(Fe₂O₃)をつくる。
遷移元素
周期表の真ん中あたり(3〜12族)
│ 3 4 5 6 7 8 9 10 11 12 │ ← この横長の金属ゾーン
特徴のイメージ
・キラキラした金属ばかり ✨
・色のついたイオンをつくる 🎨
・複雑な形の錯イオンをつくる 🔷
・電子が動きやすくて触媒になる ⚙️
・酸化数がコロコロ変わる ↗↘
例:鉄(Fe)のイメージ
Fe → 2価(Fe²⁺) → ちょっと電子を失う
Fe → 3価(Fe³⁺) → もっと電子を失う
荷電子(価電子)と不対電子
原子の最外殻にある電子は化学反応や結合に関わり、価電子と呼ばれる。そのうちペアになっていない電子は不対電子で、共有結合をつくる際に重要な役割を果たす。原子価は原子がつくる結合の数を表し、共有結合では不対電子の数が原子価になる。イオン結合では、正の原子価は放出した電子の数、負の原子価は受け取った電子の数で決まる。原子番号が大きくなるほど複数の原子価を示す元素が増え、硫黄(S)は2価(H₂S)、4価(SO₂)、6価(SO₃)などをとる。水素(H)は常に1価である。
価電子と不対電子
原子の外側の殻
●● ← ペア(対電子)
● ← ひとりぼっち(不対電子)
不対電子のイメージ
● ← 他の原子と手をつなぎたがる
→ 共有結合をつくる
原子価
・共有結合の場合
不対電子の数 = 手の数(=原子価)
・イオン結合の場合
+原子価 → 手放した電子の数
−原子価 → 受け取った電子の数
硫黄(S)のイメージ
S:手が2本 → H₂S
S:手が4本 → SO₂
S:手が6本 → SO₃
水素(H)
H:手はいつも1本だけ
以下の動画でもお楽しみ下さい。
化学結合のしくみ
共有結合
原子同士が不対電子を出し合って共有することで共有結合ができる。共有された電子は両方の原子に属し、結果として希ガスのような安定した電子配置に近づく。18族の希ガスはすでに安定しているためほとんど反応しないが、その他の原子は安定構造を目指して電子を共有する。原子価は「共有できる不対電子の数」で決まり、ハロゲンは1価、酸素は2価、窒素やリンは3価(リンは5価もとる)、炭素は4価、水素は1価となる。
共有結合
原子A ● ● 原子B
↑ 共有する電子対 ↑
→ 不対電子どうしが手をつなぐイメージ
→ 希ガスみたいに安定した形を目指す
原子価のイメージ
F:● → 1本の手
O:●● → 2本の手
N:●●● → 3本の手
C:●●●● → 4本の手
H:● → 1本の手
配位結合(座標結合)
共有結合の一種に配位結合(座標結合)があり、これは電子対を片方の原子だけが提供してできる結合である。アンモニウムイオン NH₄⁺ は NH₃ の非共有電子対に H⁺ が結合したもので、オキソニウムイオン H₃O⁺ も同様に H₂O の非共有電子対に H⁺ が結合してできる。不対電子の数より結合が1つ多くなるのが特徴で、この仕組みは金属イオンと配位子が結合する錯イオンにも見られる。
配位結合(座標結合)
原子A:●●(電子対を持っている)
原子B: (電子なし)
A →→→ B に電子対を“あげる”イメージ
錯イオンと配位子
金属イオンに分子や陰イオンが電子対を提供して結合したものを錯イオンと呼び、金属に結合する分子・イオンを配位子という。[Ag(NH₃)₂]⁺(ジアンミン銀(I))、[Cu(NH₃)₄]²⁺(テトラアンミン銅(II))、[Fe(CN)₆]⁴⁻(ヘキサシアノ鉄(II)酸イオン)などが例で、荷電数は金属イオンの電荷と配位子の電荷の合計で決まる。
例:
NH₃ + H⁺ → NH₄⁺
H₂O + H⁺ → H₃O⁺
錯イオンと配位子
NH₃ →→→
[ Ag⁺ ] ←←← NH₃
NH₃ →→→
→ 金属イオンのまわりに配位子がくっつく
→ 電子対を“差し出して”結合する
例
[Ag(NH₃)₂]⁺
[Cu(NH₃)₄]²⁺
[Fe(CN)₆]⁴⁻
エノール
カルボニル化合物(アルデヒド・ケトン)はケト型とエノール型の平衡で存在し、α位の水素が酸性であるためエノール型に変わりやすいが、多くの場合はケト型が優勢である。
ケト型:
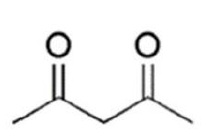
エノール型:
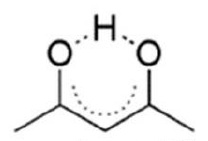
→ ふだんはケト型が多い
イオン結合
陽イオンと陰イオンが静電気力(クーロン力)で引き合う結合がイオン結合である。金属は電子を失って陽イオンになり、非金属は電子を受け取って陰イオンになる。1族元素は1価の陽イオン、2族は2価の陽イオン、ハロゲンは1価の陰イオンをつくる。
Na → e⁻ を手放す → Na⁺
Cl ← e⁻ を受け取る ← Cl⁻
Na⁺ + Cl⁻
↓ 引き合う(クーロン力)
NaCl
水素結合
電気陰性度の大きい原子(O, N, F)に結合した水素が、別の分子の陰性原子と引き合う強い分子間力が水素結合である。H₂O、NH₃、HF などが代表例で、水の沸点が高いのは水素結合が強いためである。
H–O···H–O···H–O
↑ここが水素結合
→ O, N, F と結合したHが、別の分子の陰性原子に引き寄せられる
→ 水の沸点が高い理由
水和(溶媒和)
溶液中でイオンや分子の周りに溶媒分子が強く引きつけられて集まる現象を溶媒和といい、溶媒が水の場合は水和と呼ぶ。水は極性が大きいためイオンを強く安定化する。
Na⁺ を水が取り囲む
○ ○
○ Na⁺ ○
○ ○
水分子の向きがそろってくっつく
極性
共有電子対が電気陰性度の大きい原子に偏ることで電荷の偏りが生じ、これを極性という。HCl では Cl 側が負、H 側が正になり、H₂O では O が負、H が正になる。極性は沸点や溶解性などの性質に影響する。
H — Cl
→ 電子がCl側へ偏る
H:+
Cl:−
→ 電荷の偏りが性質に影響
金属結合
金属結合では金属原子が価電子を放出し、自由電子を全体で共有する。自由電子が動き回るため電気をよく通し、熱も伝わりやすく、金属特有の光沢や延性もこの仕組みで説明できる。
金属原子:○ ○ ○ ○
自由電子: ・・・・・・(全体を動き回る)
→ 電気・熱をよく通す
→ 光沢・延性が生まれる
構造式(簡略構造式)
構造式(簡略構造式)は複雑な分子を簡単に表すための書き方で、C–H結合は省略し、炭素同士の結合は線で表す。二重結合・三重結合は線を2本・3本で描く。たとえば CH₃–CH₂–OH は –CH₂–OH のように簡略化して書くこともある。
CH₃–CH₂–OH
↓ C–Hは省略
–CH₂–OH
→ 線で炭素骨格を表す
以下の動画でもお楽しみ下さい。
